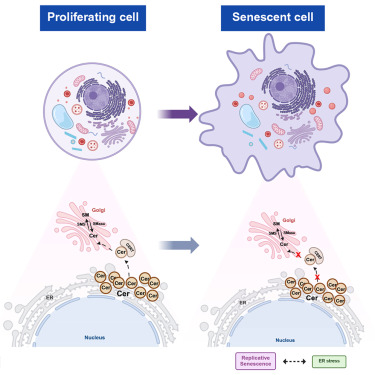
脂质作为空间调控的信号分子发挥作用。它们的生物活性不仅取决于其丰度,还取决于其亚细胞定位。神经酰胺便是这一原理的典型例证:线粒体神经酰胺的积累会促进细胞凋亡,然而神经酰胺区室化如何调控其他细胞命运程序仍不清楚。本文中,我们证实复制性衰老不仅由神经酰胺水平升高所定义,还由神经酰胺转运紊乱所定义,后者驱动神经酰胺在内质网(ER)的积累。我们发现,通过CERT介导的ER到高尔基体的神经酰胺转运受损是衰老相关鞘脂重塑的关键调控节点。在功能上,干扰神经酰胺转运会模拟衰老的脂质和表型特征,揭示了脂质转运是决定细胞命运的关键因素。通过将内质网定位的神经酰胺积累与内质网应激信号联系起来,这项工作揭示了脂质空间组织与衰老程序之间的联系,突出了细胞器解析的脂质代谢作为衰老生物学中一个可靶向的轴。
🔗 https://www.cell.com/cell-chemical-biology/abstract/S2451-94562600073-5
