科学界普遍认为,某些胆固醇运输颗粒(例如低密度脂蛋白胆固醇 (LDL-C))的高水平在动脉粥样硬化性心血管疾病 (ASCVD) 的发展中起着重要作用。然而,一部名为《胆固醇密码》( The Cholesterol Code)的纪录片最近对这种关于心脏病发病机制的基础性理解提出了挑战,并在社交媒体上引发了关于我们对心血管健康认知的激烈辩论。这部影片与一个名为“公民科学基金会”(Citizen Science Foundation , CSF) 的组织有关,该组织开展由私人捐款资助的独立研究。影片认为,即使 LDL 胆固醇水平非常高,也未必总是意味着 ASCVD 风险。他们这一颇具争议的假设的核心是他们称之为“瘦体重高反应者”(LMHR) 的人群:这些人采用低碳水化合物、高脂肪的生酮饮食后,LDL-C 水平显著升高,但却保持着一组特定的其他有益代谢指标。这种特定表型是否存在本身就值得商榷,但该假设真正具有争议性的部分在于,它认为血清低密度脂蛋白胆固醇(LDL-C)可能并非低密度脂蛋白胆固醇血症(LMHR)患者发生动脉粥样硬化性心血管疾病(ASCVD)的主要驱动因素。这场争论远非学术探讨,它触及了我们对心血管风险认知的核心,并对数十年来严谨的科学研究提出了挑战。在深入探讨细节之前,有必要明确指出核心问题:动脉粥样硬化是由循环中载脂蛋白B(apoB)颗粒的数量驱动的,无论这些颗粒升高的原因或方式如何,这种关系都成立。问题的关键不在于LMHR在代谢上是否与其他人群不同,而在于他们是否不受这种生物学规律的影响。
开始之前,我想快速提两点:
首先,我们意识到接下来的讨论会涉及一些生物化学知识,这是无法避免的。要理解CSF提出的论点,以及我们提出的反驳论点,就必须超越片面的宣传和社交媒体上的讨论。我们力求精简不必要的文字,同时保留内容的深度和严谨性。我们鼓励所有人,无论您是赞同、反对、犹豫不决,还是感到困惑,都认真思考这些材料。
其次,数十年来卫生部门的误导性指导,加上科学(一个探索的过程)与倡导(服务于特定议程)日益交织,加剧了公众对科学机构的普遍不信任,尤其是在涉及人类健康的问题上。在许多情况下,这种怀疑是可以理解的,甚至是合理的。然而,虽然盲目接受每一种医学教条是天真的,但完全否定科学共识则是一个更大的错误,而且会带来严重的后果。
好的,让我们开始吧。
了解脂质和脂蛋白
胆固醇是人体每个细胞必需的分子。它是细胞膜的重要组成部分,也是胆汁酸和多种激素的前体。肝脏是血浆中胆固醇的主要生产者,而大脑则自行合成胆固醇。膳食来源的胆固醇含量则少得多。肝脏合成的胆固醇必须被运输到身体的其他部位,但这项任务面临着一个根本性的挑战:胆固醇不溶于水,因此无法在血液中自由流动。
脂蛋白正是在这里发挥作用。你可以把脂蛋白想象成特殊的运输工具,或者说是潜艇,它们将脂溶性分子包裹在由蛋白质和磷脂组成的亲水性水溶性外壳中,从而在血液中运输这些分子。除了胆固醇之外,脂蛋白运输的主要分子还包括甘油三酯,也就是脂肪,脂肪是人体储存能量的主要形式。
脂蛋白颗粒的大小和密度各不相同,从体积大、密度低(因此漂浮性强)、富含脂质的乳糜微粒到体积小、脂质含量低的高密度脂蛋白(HDL),如图1所示。不同类型的脂蛋白发挥着不同的作用,有些脂蛋白还可以转化为其他脂蛋白。例如,一些极低密度脂蛋白(VLDL)在血液中会逐渐转化为低密度脂蛋白(LDL),这是因为其核心甘油三酯和表面磷脂在酶的作用下被移除,供人体利用。
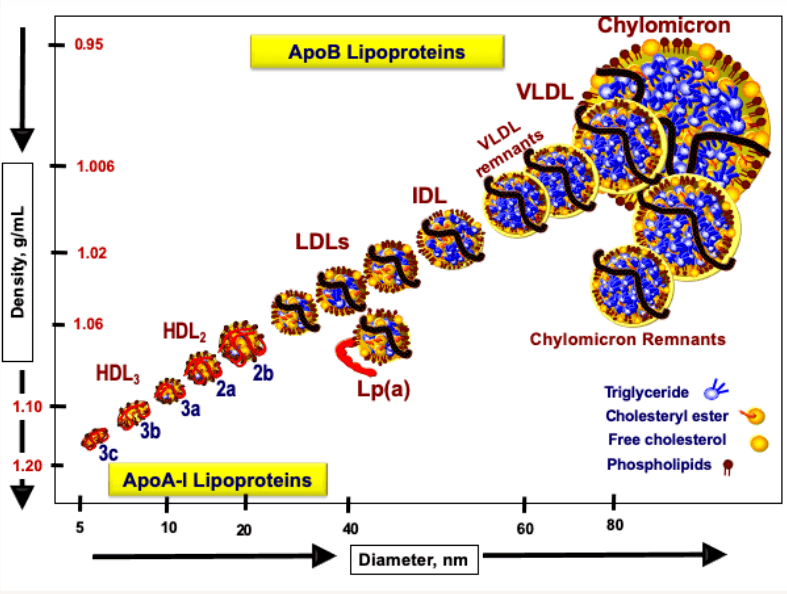
然而,至关重要的是,只有少数几种脂蛋白能够进入动脉壁并引发动脉粥样硬化。具体而言,致动脉粥样硬化脂蛋白是指那些被单分子载脂蛋白B (apoB)包裹的脂蛋白。含apoB的脂蛋白包括中间密度脂蛋白(IDL)、低密度脂蛋白(LDL)、极低密度脂蛋白(VLDL)、乳糜微粒和乳糜微粒残余物。但由于LDL颗粒在血浆中的停留时间远长于其他含apoB的脂蛋白,因此循环中绝大多数(约90%至95%)的apoB都来源于LDL。由于apoB主要存在于LDL中,且每个LDL颗粒仅含有一个apoB分子,因此血浆apoB水平实际上可以作为LDL颗粒数量的指标,进而大致反映循环中致动脉粥样硬化脂蛋白的总数。
(过去估算低密度脂蛋白(LDL)颗粒数量的方法是测量这些颗粒所携带的总胆固醇质量,即“LDL胆固醇”,其依据是平均每个LDL颗粒含有可预测量的胆固醇。这种方法的缺陷在于,在相当一部分人群中,LDL-C与LDL颗粒数量之间的关系存在偏差,导致LDL-C可能低估或高估真实风险。但现在我们可以直接测量载脂蛋白B(apoB),从而获得比单独使用LDL-C更准确的评估动脉粥样硬化性心血管疾病(ASCVD)风险的方法)
LMHR假说
那么,“瘦体重超敏反应者”的概念又该如何解释呢?CSF 已经识别出一种他们认为的特定表型:这些人在采用低碳水化合物或生酮饮食后,会表现出独特的代谢反应,其特征是三种脂质标志物。首先,他们的低密度脂蛋白胆固醇 (LDL-C) 水平显著升高,通常超过 200 mg/dL,有时甚至超过 400 mg/dL。相比之下,美国心脏协会建议将 LDL-C 水平控制在 100 mg/dL 以下,对于动脉粥样硬化性心血管疾病 (ASCVD) 高风险人群,则应控制在 55 mg/dL 以下。<sup> 3 </sup> LDL-C 的升高与血浆载脂蛋白 B (apoB) 浓度的增加相对应。<sup> 4,5</sup>这三种标志物中的第二个特征是高密度脂蛋白胆固醇 (HDL-C) 水平异常升高,通常高于 80 mg/dL。第三,甘油三酯水平保持相对较低,通常低于 70 mg/dL。这种脂质表型尤其引人注目,因为它与传统的血脂异常模式不同,在传统的血脂异常模式中,LDL-C 升高通常伴随甘油三酯升高和HDL-C相对较低。
CSF进一步指出,除了血脂谱之外,这些个体还具有其他几个共同特征。他们通常体型偏瘦,男性体脂率通常低于15%,女性低于25%,身体活跃,并且根据空腹血糖、胰岛素敏感性和炎症标志物等常规指标判断,代谢健康。许多人是耐力运动员或定期进行力量训练。
根据CSF的假设,这种表型代表了一种独特的代谢适应,以适应低碳水化合物、高脂肪的营养,而非病理状态。他们指出,生酮饮食下LDL-C的急剧升高仅见于BMI低于25 kg/m²的瘦人,而非超重或肥胖人群<sup> 6 </sup>。他们提出,这些个体能够更有效地动员和利用脂肪供能,从而形成其独特的血脂谱。基于此观点,LDL-C升高被认为是脂肪代谢增强的标志,可能与独特的心血管风险特征相关。一些支持者更进一步,由此推断高LDL-C水平可以忽略不计。
“脂质能量模型”
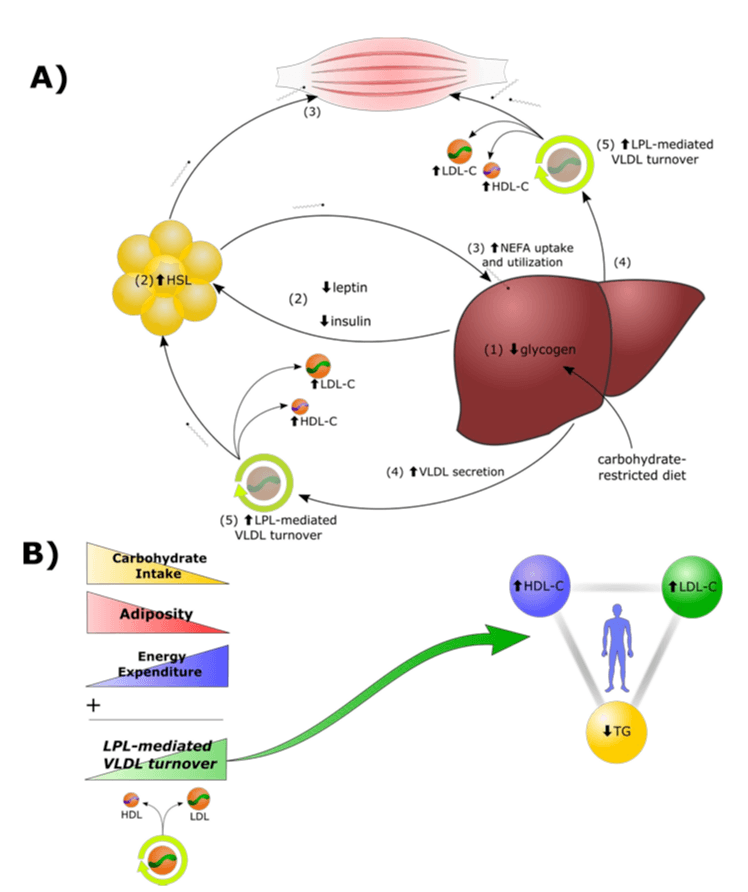
为了解释这种可能的低能量低碳水化合物反应(LMHR)现象,脑科学基金会(CSF)开发了所谓的“脂质能量模型”,该模型提出了一系列复杂的代谢适应反应,以应对碳水化合物限制(图2)。
当低代谢高反应性(LMHR)个体限制碳水化合物摄入时,其肝糖原储备(葡萄糖的储存形式)会耗竭,从而导致身体更多地依赖脂肪酸而非葡萄糖作为能量来源。这种转变据称会导致基础胰岛素和瘦素水平降低,进而增加脂肪细胞中的脂肪分解,即甘油三酯分解为非酯化脂肪酸(NEFA)并释放到血液中的过程。随着循环中NEFA的增多,肝脏会吸收更多NEFA,并将其重新合成甘油三酯。随着肝脏甘油三酯合成的增加,富含甘油三酯的极低密度脂蛋白(VLDL)颗粒的分泌也随之增加。这些VLDL随后在外周组织中迅速代谢,甘油三酯通过一种名为脂蛋白脂肪酶的酶的作用被清除。随着甘油三酯从VLDL中被清除,这些颗粒转化为低密度脂蛋白(LDL),最终导致低密度脂蛋白胆固醇(LDL-C)水平升高,至少该模型是这么认为的。
CSF认为,这一过程与导致低密度脂蛋白胆固醇(LDL-C)升高的其他疾病(例如家族性高胆固醇血症)有着本质区别。他们指出,在低密度脂蛋白胆固醇血症患者(LMHR)中,高LDL-C水平反映了一种高周转状态,在这种状态下,脂蛋白向组织输送更多能量,因此与LDL-C水平同样升高的其他疾病相比,其在动脉壁上的积聚程度可能较低。他们还提出,这些个体持续存在的低甘油三酯和高高密度脂蛋白胆固醇(HDL-C)水平表明其脂质代谢高效且具有保护性适应机制。
然而,正如我们将要详细探讨的那样,该模型本身及其所依据的证据都存在重大问题。虽然在某些低碳水化合物饮食者中观察到的这种脂质模式似乎是真实的,但对其意义的解读以及为解释这种模式而提出的机制性解释都面临着严峻的科学挑战。
审查证据
LMHR 假说的大部分所谓支持都来自纪录片《胆固醇密码》中重点介绍的两项相关研究。
这项主要研究是一项为期一年的前瞻性观察性队列研究,重点关注低密度脂蛋白胆固醇(LMHR)患者动脉粥样硬化的发展。 <sup> 5,8</sup>该研究旨在利用冠状动脉计算机断层扫描血管造影(CCTA)监测100名接受生酮饮食的LMHR或“近LMHR”个体冠状动脉粥样硬化的发展和进展。受试者需在研究开始前至少两年坚持生酮饮食,且低密度脂蛋白胆固醇(LDL-C)水平升高(至少190 mg/dL,参与者中位数约为260 mg/dL),同时高密度脂蛋白胆固醇(HDL-C)水平也相对较高(至少60 mg/dL)。
研究人员报告称,一年内,斑块进展(非钙化斑块体积中位数进展为 5.6 mm³)与基线载脂蛋白 B (apoB) 水平、apoB 变化或总低密度脂蛋白胆固醇 (LDL-C) 暴露量无关,而基线斑块负荷与后续斑块进展相关。换言之,主要结论是斑块会促进斑块形成,而 apoB 和 LDL-C 在该队列中不能预测短期斑块进展。
即使仅从表面上看,这些结果也无法解答所提出的问题,因为它们考察的时间尺度错误。动脉粥样硬化风险是载脂蛋白B(apoB)脂蛋白累积暴露量的函数,通常被概念化为apoB浓度随时间变化的积分。因此,在一个既往暴露存在数十年异质性的队列中,仅进行一年的观察,从结构上来说无法检测到其试图测量的效应。相关的问题不是apoB能否预测一年内的斑块变化,而是多年持续暴露是否会增加累积疾病负担。由于研究设计的原因,这项研究无法回答这个问题。
更具参考价值的研究设计应包含一个对照组,该组受试者具有相似的高LDL-C水平,但血脂异常特征更为典型,例如低HDL-C和高甘油三酯。如果一年时间足以评估高LDL-C是否驱动低密度脂蛋白胆固醇(LMHR)患者的动脉粥样硬化性心血管疾病(ASCVD)进展,那么一个合适的非LMHR、高LDL-C对照组在同一时期内的疾病进展应明显高于仅基于其其他风险因素所预测的进展。然而,研究人员并未纳入此类对照组。这一疏漏使得我们难以将该研究结果解读为LMHR表型与更典型的严重LDL-C升高形式存在显著差异的证据。即使采用这种设计也并非完美,因为这些人群除了血脂谱之外,在其他重要方面仍存在差异,例如血压和胰岛素抵抗,而这两者都会影响ASCVD风险。
尽管可能需要更长时间才能得出结果,但一个更强有力的对照组应该是低密度脂蛋白胆固醇(LDL-C)水平较低或中等,但其他风险因素与低密度脂蛋白胆固醇高危人群(LMHR)一致的个体。如果LMHR人群中LDL-C升高带来的风险确实消失,那么他们的斑块进展应该不会比这个健康对照组更严重。然而,本研究仍然没有招募到这样的对照组。
为了部分弥补这一不足,作者引用了2024年发表的一项横断面研究,该研究纳入了匹配的对照组。<sup> 9</sup>该研究比较了80名低密度脂蛋白胆固醇(LMHR)患者(平均遵循生酮饮食4.7年)与来自迈阿密心脏队列研究的对照组,对照组在年龄、性别、种族、高脂血症、糖尿病、高血压和吸烟状况方面与LMHR患者相匹配。两组的低密度脂蛋白胆固醇(LDL-C)水平差异显著,LMHR组(本文中称为“生酮”组)的平均LDL-C水平为272 mg/dL,部分个体甚至高达591 mg/dL,而对照组的平均LDL-C水平为123 mg/dL。该研究利用冠状动脉CT血管造影(CCTA)数据比较了两组的冠状动脉斑块情况,并分析了LDL-C水平与斑块水平的相关性。结果显示,两组的冠状动脉斑块负荷无差异,LDL-C水平与CCTA冠状动脉斑块之间也无相关性。但问题仍然存在:LMHR 中 LDL-C 升高是否比传统血脂异常的风险更小?
如上所述,仅分析主要研究就足以对结果产生重大质疑,因为最明显的对照组被忽略了,而且研究持续时间太短,不足以显示动脉粥样硬化从基线开始的进展。但当我们转向相关研究时,其他几个缺陷也显露出来。
首先,这项研究严格来说是横断面研究,这意味着数据仅在单一时间点收集,用于对各组进行一次性比较。研究没有追踪任何指标随时间的变化,而追踪这些指标本可以更深入地了解生酮饮食如何影响低密度脂蛋白胆固醇(LDL-C),以及LDL-C升高与动脉粥样硬化性心血管疾病(ASCVD)发展之间的关系。动脉粥样硬化是人体动脉在数年甚至数十年间累积暴露于载脂蛋白B(apoB)脂蛋白的结果,而非某一天的血脂水平。低密度脂蛋白胆固醇(LMHR)组的受试者平均年龄为55.5岁,根据研究方案,他们在开始生酮饮食前LDL-C水平相对正常(122 ± 36 mg/dL),且未检测出家族性高胆固醇血症。这意味着,在生酮饮食诱导高胆固醇血症的4.7年之前,生酮饮食组的受试者可能已经经历了长达50年的中等程度的apoB暴露。相反,迈阿密心脏研究中对照组受试者在与酮症组匹配时同样较高的低密度脂蛋白胆固醇(LDL-C)水平,可能反映了他们数十年来长期暴露于如此高的LDL-C水平。这些患者在横断面研究时的载脂蛋白B(apoB)水平无法反映他们截然不同的暴露史,这很可能解释了迈阿密心脏研究中对照组动脉粥样硬化程度较酮症组更为严重的原因。
其次,匹配过程存在不足。虽然该研究匹配了年龄、性别、种族和吸烟状况等传统风险因素,但未能考虑其他可能影响心血管风险的关键变量。自愿坚持严格生酮饮食近五年的人群,在体力活动、社会经济地位、整体饮食质量以及许多其他生活方式因素(例如,健康用户偏差)方面,可能与普通人群存在显著差异。这些变量均未进行匹配或控制,但任何一个变量都可能影响研究结果。此外,生酮组除了血脂谱之外,还表现出显著的基线优势。与迈阿密心脏研究的参与者相比,他们的BMI更低(22.5 vs. 25.8),炎症标志物更低(hsCRP:0.5 vs. 0.7 mg/L;P = 0.007),HDL-C更高,甘油三酯更低。虽然这些差异可能是所谓的低密度脂蛋白胆固醇(LMHR)表型的一部分,但它们仍然使得我们无法分离出LDL-C升高对心血管风险的具体影响。
因此,与其说低密度脂蛋白胆固醇(LMHR)人群对生酮饮食有特殊反应,使高LDL-C水平变得无害,不如说更简单的解释是:高LDL-C导致的心血管风险在不同个体间是一致的,但迈阿密心脏队列的动脉粥样硬化性心血管疾病(ASCVD)风险升高至与LMHR人群相似的水平,是由于他们长期暴露于高载脂蛋白B(apoB)水平、代谢健康状况较差、炎症水平较高,以及可能较差的体力活动、饮食和社会经济地位所致。换句话说,在横断面研究时,LMHR组除了LDL-C水平之外,在其他诸多方面都比对照组更健康,而这些优势共同抵消了其较高血脂水平带来的负面影响。
仔细审视机制模型
尽管用于支持LMHR假说的数据存在问题,但“脂质能量模型”在理论上仍然站得住脚吗?仔细审视后,就连这一机制基础也开始瓦解。
任何可行的模型都必须解释载脂蛋白B(apoB)水平升高的幅度。脂质能量模型在所有三个方面都存在缺陷:它无法解释观察到的颗粒数量增加,与定义该表型的低甘油三酯水平相矛盾,并且缺乏对其关键步骤的直接实验验证。
如前所述,该模型的核心是脂肪分解增加导致肝脏甘油三酯合成增加,以及极低密度脂蛋白(VLDL)的分泌和周转增加,最终导致低密度脂蛋白胆固醇(LDL-C)水平升高。然而,这种解释存在几个根本性问题。首先,脂肪细胞脂肪分解后肝脏增加甘油三酯合成的程度尚不清楚,因为脂肪细胞释放的非酯化脂肪酸(NEFA)会在几分钟内分布到组织中,目前尚不清楚有多少NEFA能够到达肝脏并达到足以刺激甘油三酯合成和分泌显著增加的水平。更重要的是,当肝脏产生更多甘油三酯时,它主要通过增加甘油三酯负载来增大VLDL颗粒的大小,但并不会显著增加VLDL颗粒的分泌数量。这意味着甘油三酯分泌增加并不会显著增加载脂蛋白B(apoB)脂蛋白的总血浆浓度(apoB是驱动动脉粥样硬化的关键变量),因此无法解释在所谓的低脂高胆固醇血症(LMHR)患者中观察到的apoB水平的显著升高。<sup> 10</sup>
此外,即使极低密度脂蛋白(VLDL)颗粒数量大幅增加,我们也应该观察到血浆甘油三酯水平升高,因为VLDL中的甘油三酯是血清总甘油三酯浓度的主要来源。但需要注意的是,低甘油三酯水平是低脂高胆固醇血症(LMHR)的标志性特征之一。一些支持该模型的人认为,这些患者体内高密度脂蛋白胆固醇(HDL-C)水平高表明甘油三酯周转率高,从而可以解释低甘油三酯水平,但目前尚无证据表明情况确实如此——即便如此,也无法弥补该模型的缺陷,因为VLDL颗粒数量高仍然会导致血清甘油三酯稳态水平升高。这种解释感觉像是不断转移目标,对核心论点的每一次反驳都对应着一个新的、未经检验的解释。更合理的解释是,高HDL-C水平是由于HDL颗粒吸收了更多外流胆固醇所致,而细胞胆固醇合成增加是饱和脂肪摄入增加的已知后果。
最后,该模型提出高LDL浓度是由于VLDL的快速代谢所致,VLDL在脂蛋白脂肪酶的作用下,甘油三酯含量降低,最终转化为LDL。然而,迄今为止,LMHR假说的支持者尚未提供任何证据表明LMHR具有较高的VLDL脂解率或升高的脂蛋白脂肪酶活性,而这两点对于该模型的成立至关重要。VLDL向LDL的转化对于脂质能量模型的合理性至关重要,但尽管已有相应的检测方法,却从未在此背景下进行过实验验证。
这些患者低密度脂蛋白胆固醇(LDL-C)升高的一个更简单的解释是以下两种情况之一或两种:1)肝脏生成和分泌富含胆固醇的大颗粒低密度脂蛋白(LDL)增加;或 2)由于饱和脂肪诱导的低密度脂蛋白受体抑制和胆固醇合成增加,导致肝脏从血浆中清除载脂蛋白B(apoB,主要是LDL)的能力下降。然而,关键问题并非这些患者体内apoB升高的原因,核心问题依然存在。
关键问题
这场争论的核心问题并非低密度脂蛋白胆固醇血症患者是否具有独特的代谢特征,也并非其高LDL-C水平的产生机制是否与其他类型的高胆固醇血症不同。根本问题在于,无论LDL-C和载脂蛋白B水平升高的原因或机制如何,持续升高的LDL-C和载脂蛋白B水平是否会导致这些个体发生动脉粥样硬化。
如下图(图3 )所示,数十年的研究一致表明,载脂蛋白B(apoB)脂蛋白是动脉粥样硬化的致病因素。其机制并非抽象概念。它始于apoB颗粒在动脉壁的滞留,随后这些颗粒发生修饰,被巨噬细胞摄取,并引发局部炎症反应,最终导致斑块形成。关键在于,上述每个步骤都与颗粒数量和累积暴露量密切相关。动脉壁不会“探究”apoB升高的原因,而是对进入动脉壁的颗粒数量及其停留时间做出反应。因此,任何声称某种特定表型不受此影响的说法,都必须从动脉生物学层面解释为何这一过程会被中断。然而,目前尚未有这样的解释。
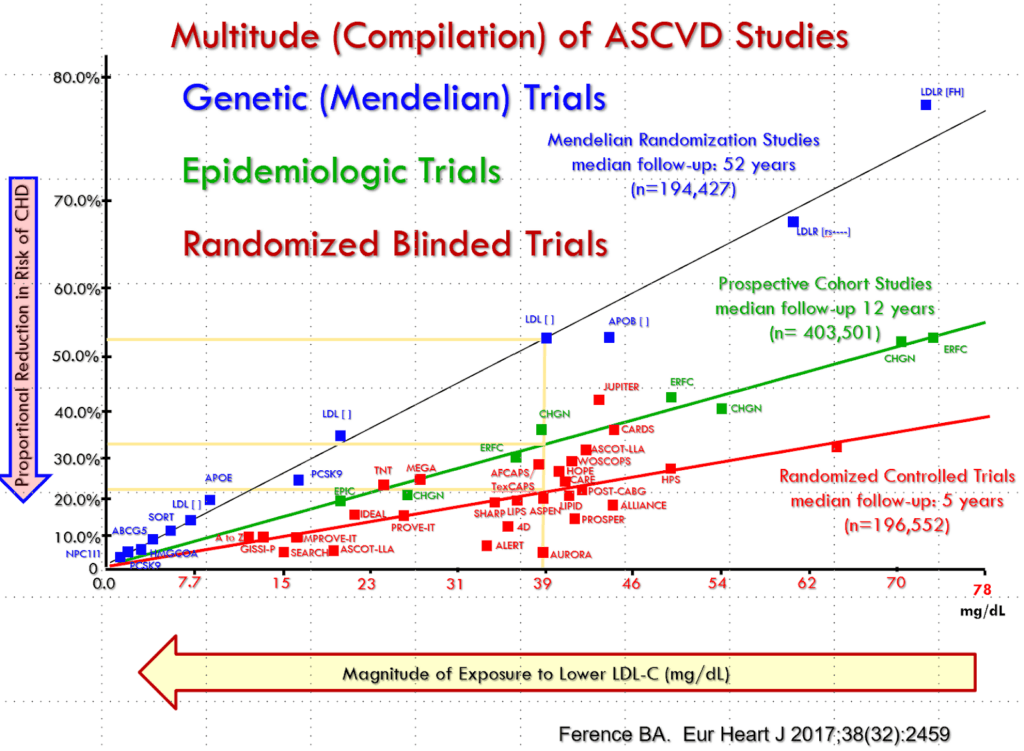
这些结论得到了数百项人群研究、遗传学研究(例如孟德尔随机化)、降低低密度脂蛋白胆固醇(LDL)药物的随机对照试验以及基础科学研究的支持。此外,如果LDL是致病因素,那么除非有机制能够打破这种因果关系,否则它在所有代谢背景下都必须是致病因素。例如,在家族性高胆固醇血症中,载脂蛋白B(apoB)水平升高具有致动脉粥样硬化作用(详见下文),无论其潜在机制是LDL受体功能缺陷、PCSK9(一种降解这些受体的酶)的改变,还是apoB合成本身缺陷所致。相反,多种降低载脂蛋白B的干预措施可以减少ASCVD的进展和事件,其机制包括通过减少胆固醇合成(他汀类药物、贝培多酸)来增加LDL受体表达,或抑制肠道对肝胆排泄或膳食胆固醇的吸收(依折麦布),降低肝脏LDL受体周转率(PCSK9抑制剂),或增加肝脏LDL受体活性(增加膳食多不饱和脂肪酸与饱和脂肪酸的比例)。
在所有情况下,风险变化都与载脂蛋白B浓度的变化相关,而与实现这种变化的机制无关。因此,举证责任在于那些声称低代谢高危人群(LMHR)能够摆脱这种生物学规律——即它们是这条已被广泛认可的规则的例外——的人。两项设计不佳的观察性队列研究不足以反驳如此大量的证据,尤其是在与之竞争的机制论证本身就站不住脚的情况下。
换句话说,Keto CTA 研究的问题远不止缺乏对照组和研究时间短。鉴于风险与累积 apoB 暴露量成正比,在一个相对年轻、低负担人群中未观察到短期相关性,并不能否定因果关系。这恰恰是完全因果模型下的预期结果。
事实上,(现已撤稿并以预印本形式重新发表的)Keto CTA 研究的作者也承认了这一点:针对对 Keto CTA 研究的质疑,他们表示:“此外,我们的结果与载脂蛋白 B 在动脉粥样硬化中的因果作用相符,正如我们在之前的出版物中公开承认和支持的那样。”<sup> 12</sup>
有了这一让步,争议的核心范围就大大缩小了。问题不再是含载脂蛋白B的脂蛋白是否是动脉粥样硬化的致病因素,而是是否存在某种特定的代谢环境能够显著减弱这种因果关系。这需要更高的证据标准。证明效应修饰与质疑因果关系本身有着本质的区别,它需要可靠的长期数据来证明,同等水平的载脂蛋白B暴露会导致不同的临床结局。目前尚无此类证据。因此,承认载脂蛋白B是致病因素,同时暗示某个亚组人群不受其影响,这种推断缺乏证据支持,而只是一个未经检验的假设。
家族性高胆固醇血症的教训
LMHR假说的支持者经常试图将他们的研究人群与家族性高胆固醇血症(FH)患者区分开来。FH是一组遗传性疾病,会导致极高的低密度脂蛋白胆固醇(LDL-C)水平和动脉粥样硬化性心血管疾病(ASCVD)的早期发生。许多FH患者的LDL受体存在基因缺陷,这些受体负责通过肝脏清除血液循环中的LDL。因此,他们清除LDL的效率低下,导致LDL-C和载脂蛋白B(apoB)水平显著升高。LMHR假说的支持者认为,FH代表脂质代谢功能障碍,而LMHR患者的LDL-C水平升高是“功能性的”,他们列举了两组人群之间的几个区别作为证据:
- 低密度脂蛋白胆固醇 (LMHR) 患者仅在生酮饮食时 LDL-C 升高,在混合宏量营养素饮食时 LDL-C 正常,而家族性高胆固醇血症 (FH) 患者无论饮食组成如何,LDL-C 都会升高。
- FH 患者的 LDL 水平升高,与 BMI 无关,而 LMHR 患者的 LDL 水平与 BMI 呈负相关。
- FH 患者的 HDL-C 和甘油三酯水平各不相同,而 LMHR 患者的 HDL-C 始终高于 80 mg/dL,甘油三酯始终低于 70 mg/dL。
然而,即使这些受试者体内高 apoB 水平是燃料分配适应性反应的结果,但这并不意味着它是良性的“功能性”的,就像胰岛素抵抗并非“功能性”的,因为它是细胞对细胞内能量过载的适应性反应一样。
这些区分方法中有些还存在其他缺陷。例如,低密度脂蛋白胆固醇(LDL-C)与体重指数(BMI)在低代谢高危人群(LMHR)中呈负相关,但这并不能解释在给定BMI值下身体成分可能存在的显著差异,因此无法反映受试者的真实代谢状态。
“功能性”和“功能障碍性”脂质代谢之间的区别无关紧要。在家族性高胆固醇血症中,载脂蛋白B (apoB) 可通过多种机制升高,包括低密度脂蛋白受体缺陷、PCSK9 变异或 apoB 合成改变。无论何种情况,风险都与 apoB 浓度相关,而非与其产生机制相关。动脉粥样硬化的基本机制,即含 apoB 的脂蛋白在动脉壁的积聚,并不取决于这些颗粒升高的原因。如果你面临行刑队,射向你裸露躯干的子弹是由单发步枪、栓动步枪还是半自动步枪发射的,其实无关紧要:子弹越少越好。
对家族性高胆固醇血症(FH)患者的研究为我们提供了关于载脂蛋白B(apoB)和低密度脂蛋白胆固醇(LDL-C)在动脉粥样硬化中因果作用的最有力证据之一。除了上述差异外,低密度脂蛋白高胆固醇血症(LMHR)假说的支持者还指出最后一个区别:虽然我们知道FH患者具有较高的心血管风险,但我们尚不清楚LMHR患者的心血管风险。然而具有讽刺意味的是,这一“区别”恰恰凸显了缺乏证据表明高LDL-C水平对LMHR表型个体无害。FH的研究已持续很长时间,FH患者自出生起就暴露于高LDL-C和apoB水平。在所有病例中,动脉粥样硬化性心血管疾病(ASCVD)的进展都很缓慢。杂合子FH患者通常在30至40岁之前不会出现重大不良心脏事件,即使是纯合子FH且apoB水平极高的儿童,除极少数例外情况外,通常在出生后十年或更长时间内也不会出现不良事件,这意味着评估apoB升高带来的风险需要很长时间。多年来,许多这类患者的CTA检查结果也正常。因此,尽管LMHR假说的支持者喜欢将FH患者与LMHR患者区分开来,但他们同时也暴露了LMHR概念中或许最大的缺陷:我们根本没有足够的时间来观察LMHR特征的全部长期后果。
实际意义
为了便于讨论,我们假设低密度脂蛋白高胆固醇血症(LMHR)表型能够准确描述人群中的一小部分。虽然预防普通人群的动脉粥样硬化性心血管疾病(ASCVD)通常要求低密度脂蛋白胆固醇(LDL-C)水平低于100 mg/dL,但LMHR人群的LDL-C水平往往高出2到6倍。然而,即使某个个体看起来符合LMHR的特征,我们也无法确切地知道他是否是“真正的”LMHR,也没有确凿的证据表明,LDL-C水平升高对该人群的长期影响与其他人群有何不同。来自传统观察性研究、孟德尔随机化和随机临床试验的证据都强烈且一致地表明,载脂蛋白B(apoB)脂蛋白是动脉粥样硬化发生的驱动因素,降低apoB或其液体替代指标LDL-C可以降低动脉粥样硬化进展以及心脏病发作和中风等重大不良心血管事件的风险。
针对大量将高LDL-C与ASCVD联系起来的数据,CSF认为,由于LMHR人群的特征在大型人群数据库中较为罕见,因此不能使用普通人群的数据来推断LMHR人群的风险。虽然高apoB血症总体上并不罕见,估计每200人中就有1人患有此症,但CSF认为,即使在这些高β脂蛋白血症患者中,符合完整LMHR表型的人也并不常见。但如果这种特征真的如此罕见,那么仅仅因为缺乏针对该亚人群的证据就断定其无害,真的明智吗?apoB脂蛋白浓度过高几乎总是致动脉 粥样硬化的。因此,我们是否需要特定证据来证明,在白细胞计数低于参考范围的左撇子红发人士、匈牙利职业篮球运动员以及ALMI高于90%的国际象棋大师中,高apoB血症也具有致动脉粥样硬化的作用呢?
最终,临床医生和患者都会面临一个实际问题:当有人在低碳水化合物、高脂肪饮食中出现非常高的 LDL-C 时,我们应该怎么办?
在纪录片《胆固醇密码》中,一些负责人认为,那些警告高载脂蛋白B(apoB)对生酮饮食影响的人,实际上是想“剥夺”人们选择这种饮食方式的权利。这是一种错误的二分法,也并非我们的本意。我们中的一位(Peter)曾连续三年坚持生酮饮食,并从中获益匪浅。多年来,我们积累了大量关于生酮饮食对特定人群益处的内容,包括我们最近推出的饮食专题播客以及我们最近对Dom D’Agostino的采访。
当然,一种方法是停止生酮饮食。但另一种方法是继续这种饮食,尤其是在它能带来体重管理和改善代谢健康等益处的情况下,同时服用降脂药物将低密度脂蛋白胆固醇(LDL-C)恢复到安全范围。
第三种选择,也是一些LMHR假说支持者所暗示的,是继续维持高LDL-C水平,因为符合LMHR标准可能意味着可以免受高LDL引起的动脉粥样硬化的侵害。对于许多符合LMHR表型的人来说,这种选择似乎最具吸引力。的确,他们可能感觉良好,没有确诊ASCVD,而且许多其他指标也都不错。然而,在最后一种情况下,唯一能验证假设是否错误的方法就是等到为时已晚,ASCVD已经发生。事实上,在纪录片的结尾,一位临床团队成员在回答有关这种生存困境的问题时建议,人们应该根据动脉成像的结果来决定是否降低血脂——也就是说,只有在动脉已经受损后才采取措施预防动脉损伤。正如我们在之前的简报中讨论过的,无论你是否正在进行生酮饮食,这都是一个不必要的错误。
此处的决策框架是不对称的。避免治疗的潜在益处有限,而误判的风险却会在数年内逐渐显现,并且可能是不可逆的。动脉粥样硬化是累积性的,通常在晚期之前临床上没有明显症状。当影像学检查或症状能够检测到它时,生物学过程已经发展到相当严重的程度。相比之下,降低载脂蛋白B (apoB) 的方法众多、特性明确且通常耐受性良好。从风险管理的角度来看,预期价值计算表明,降低apoB暴露比在没有证据的情况下假设某种特定表型具有保护作用更为有利。即使在其他代谢指标都健康的情况下,将高LDL-C视为良性现象的风险也太高,而且LDL-C在动脉粥样硬化中的作用证据也过于充分,因此在没有确凿证据的情况下依赖低密度脂蛋白胆固醇降低假说是不合理的,而目前尚未提供这样的证据。
也就是说,这是否意味着代谢健康无关紧要?当然不是。代谢健康可以降低多种疾病的风险,包括动脉粥样硬化性心血管疾病(ASCVD)。反之亦然(例如,服用他汀类药物降低载脂蛋白B水平从而降低ASCVD风险,并不能自动消除内脏脂肪过多或胰岛素抵抗的风险)。但这与我们当前的讨论无关。目前已有多项研究表明,即使在没有糖尿病或其他传统心血管危险因素的情况下,低密度脂蛋白胆固醇(LDL-C)仍然与ASCVD呈单调相关。<sup>13-15</sup> 事实上,尽管尚未发表,但塔夫茨大学的迪尔德丽·托比亚斯博士已经证明,即使在具有与低密度脂蛋白胆固醇(LMHR)相似甚至更高风险特征的人群中(高密度脂蛋白胆固醇≥50 mg/dL,甘油三酯≤100 mg/dL,体重指数<25,无高血压,糖化血红蛋白<6.5%,不吸烟),较高的LDL-C水平也与全因死亡率的逐渐升高相关。16代谢健康固然重要,但无论一个人的代谢健康状况如何,都不能忽视 CVD 的主要驱动因素之一:载脂蛋白 B。
期待
低密度脂蛋白高胆固醇血症(LMHR)假说引发了关于饮食、血脂和心血管风险之间关系的宝贵讨论。它或许最终能为我们提供科学依据,帮助我们更好地理解这种不寻常的血脂谱、其发生的条件,以及它与更常见的血脂异常类型是否存在任何实质性差异。然而,要获得这些证据,需要开展一项更长期、更具针对性的心血管结局试验,但这在伦理上是不可接受的。至多,诸如体型偏瘦、体育锻炼和胰岛素敏感性等有利因素或许能够降低部分风险。尽管我们应该对新的证据持开放态度,但谨慎的做法是,无论在何种情况下,都应继续认真对待低密度脂蛋白胆固醇(LDL-C)升高的情况。
核心问题并非低密度脂蛋白胆固醇(LMHR)患者在代谢上是否异常,也并非其血脂异常的发生机制是否与传统血脂异常不同,而是长期暴露于显著升高的载脂蛋白B(apoB)含量脂蛋白是否对这类人群无害。目前尚无确凿证据表明其无害。在获得此类证据之前,人们在评估自身心血管风险时应遵循现有证据,而这些证据仍然指向同一个方向:极高的低密度脂蛋白胆固醇(LDL-C)水平是一个需要解决的问题,而不是一场需要合理化的赌博。
什么会改变我的想法
最后,我想强调一点,我认为这一点对于良好的科学思维至关重要。
我目前坚信:载脂蛋白B(apoB)脂蛋白与动脉粥样硬化存在因果关系,而且无论apoB水平升高的具体情况如何,这种关系都成立。换言之,我仍然坚信,低密度脂蛋白(LDL)及其胆固醇含量在任何情况下都是导致动脉粥样硬化的根本原因。
但对于坚定的信念,应该保持开放的态度。
这意味着,无论我对某个问题的看法多么坚定,我都可能犯错。这意味着我乐于接受新的证据。这意味着,如果证据确凿,我的信念原则上可以被推翻。我认为,这才是优秀科学家应有的思考方式。
那么,要怎样才能改变我的想法呢?
需要有清晰、可重复的证据证明,持续显著升高的载脂蛋白B水平(如我们在低密度脂蛋白血症患者中观察到的水平)的个体,在有意义的时间范围内不会发生动脉粥样硬化。不是一年,也不是两年,而是几十年。
需要设计良好的前瞻性研究,并设置适当的对照组,以证明载脂蛋白 B 水平为 150、180 或 200 mg/dL 及以上的 LMHR 个体,其斑块进展或事件发生率不会高于载脂蛋白 B 水平较低且基线风险相似的同类个体。
需要有机制证据证明,该人群中含有载脂蛋白 B 的颗粒在最重要的层面(动脉壁)上的行为有所不同。
换句话说,要使LMHR假说成立,以下两件事之一必须为真:
- 这些个体体内的含ApoB颗粒不会进入动脉壁或不会滞留在动脉壁内,或者
- 它们确实会进入细胞,但不会引发炎症以及导致斑块形成的多个步骤。
目前尚无证据支持这两种说法,而且这两种说法都需要对已建立的动脉粥样硬化生物学进行根本性的修正。
此外,还需要一个连贯的、经过实验验证的机制来解释为什么在这种特定情况下粒子数量不会转化为风险。
而且,所有这些证据都需要在时间上保持一致性、可重复性和持久性。
你或许会认为这是极高的证据门槛——你的想法没错。这是足以推翻数十年来来自遗传学、流行病学、随机对照试验和基础科学等领域汇聚的数据的证据所需的标准。因为这并非一场抽象的辩论,而是关乎人们是否应该可以安心地忽视医学界最确凿的因果风险因素之一。
在获得此类证据之前,我依然坚信:高载脂蛋白B(apoB)水平会加剧动脉粥样硬化。而极高的低密度脂蛋白胆固醇(LDL-C)水平并非可以轻视的奇特现象,而是一种必须认真对待的风险。

🔗 https://peterattiamd.com/there-is-no-safe-gamble-with-high-ldl-cholesterol/
