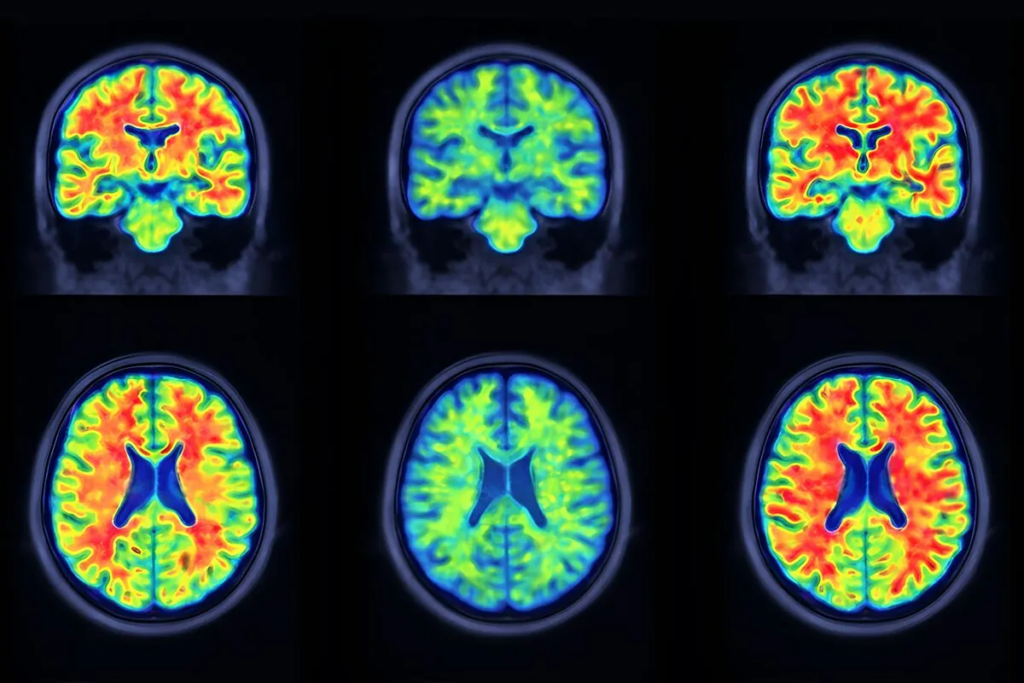
新的成像方法可以将噪声与疾病区分开来,使扫描结果更有助于追踪阿尔茨海默病的发展过程。
多年来,阿尔茨海默病的PET扫描能够显示该疾病的生物学标志——粘性淀粉样蛋白斑块和tau蛋白缠结,但一直存在一个令人沮丧的问题。扫描结果显示的这些信号并不总是能准确解释患者的实际症状。
这就是差距所在。扫描结果可能显示“阳性”,但临床医生面前的患者病情可能正在缓慢、迅速或以与影像不完全吻合的方式恶化。现在,发表在《放射学》杂志上的一项新研究表明,人工智能或许有助于弥合这种差距[ 1 ]。
中国研究人员开发了一种名为可解释对抗分解学习(ADL)的PET分析框架,旨在将阿尔茨海默病相关的病理信号与大脑的正常背景活动区分开来。实际上,它的目标是去除视觉上的“噪声”,使临床医生能够更清晰地了解真正重要的疾病信号。
由此产生了一种新的人工智能衍生生物标志物——阿尔茨海默病对抗分解 (ADAD) 评分——该评分似乎比当今一些标准的 PET 评分方法更能反映认知能力下降和神经退行性变随时间的变化。
为什么这是新出现的?
传统的PET评分工具,例如用于检测淀粉样蛋白的Centiloid和用于检测tau蛋白的CenTauRz,帮助研究人员规范了阿尔茨海默病生物学测量的方法。然而,它们将高度复杂的全脑扫描简化为一个单一的数值。
这在人口层面很有用。但当问题变得非常个人化时,它的作用就小得多:比如,此时此刻,这个大脑里发生了什么,接下来可能会发生什么?
新方法采用了不同的途径。ADL 不是将扫描结果简化为一个分数,而是创建体素级病理图——可以将其视为高度精细的热图——突出显示阿尔茨海默病相关异常可能出现的位置,同时滤除可能干扰结果解读的正常生理摄取。
作者解释说,他们的研究与目前日益兴起的定量PET测量技术发展趋势相契合,这些技术既要足够标准化,又要足够清晰,能够应用于日常临床实践。许多人工智能模型可以识别模式,但很多模型的运行方式就像黑箱一样。而研究人员的目标正是构建一种临床医生可以检查、质疑和使用的工具。
研究结果
该团队分析了一个庞大的数据集:来自阿尔茨海默病神经影像学计划、澳大利亚影像、生物标志物和生活方式研究、全球阿尔茨海默病协会互动网络以及作者所在中心的 7,457 例淀粉样蛋白 PET 扫描和 1,127 例 tau 蛋白 PET 扫描。
在外部测试中,该模型表现优异,淀粉样蛋白和tau蛋白的曲线下面积(AUC)值分别为0.94和0.98,表明其在区分临床阿尔茨海默病患者和认知功能正常个体方面具有很高的诊断区分度。但更值得关注的是其相关性。
ADAD评分与基线和纵向认知结果以及海马萎缩(即与阿尔茨海默病进展密切相关的、对记忆至关重要的大脑区域的萎缩)均存在独立关联。换句话说,该模型的输出结果与疾病随时间推移的实际表现更为吻合。
但这并不意味着旧标准已经过时。事实上,既有的量表仍然与尸检神经病理学和脑脊液生物标志物的相关性更强。但ADAD或许能提供一些不同的东西:它能更好地解读扫描结果在个体患者身上所显示的临床意义。
对于长寿医学而言,其意义远不止于放射学。该领域越来越依赖生物标志物,不仅用于疾病诊断,更用于早期发现风险、更智能地对患者进行分层,以及监测干预措施的有效性。阿尔茨海默病是对这一前景最清晰的检验之一(也是最难的检验之一)。仅仅知道是否存在病理是不够的;关键在于这种病理是否会转化为大脑衰老、功能衰退,并最终导致患者丧失独立生活能力。
在预防神经病学和个性化老龄化护理时代,一种能够更好地将脑成像与现实世界结果联系起来的生物标志物可能更具价值。它可以帮助临床医生决定哪些患者需要更密切的随访,哪些患者可能受益于新兴疗法,以及如何追踪治疗反应随时间的变化。
作者还指出,ADL 的可视化地图可以支持“临床医生与人工智能的协作”,从而可能使核医学医生、神经科医生甚至患者更容易共同解读扫描结果。
接下来会发生什么?
研究人员谨慎地表示,他们不会过分夸大研究结果。这是一项回顾性研究,他们呼吁开展前瞻性验证、更广泛的外部测试,并采用以生物标志物为中心或基于尸检结果的参考定义开展更多研究。
然而,这里的信号仍然十分引人注目。在阿尔茨海默病中,挑战从来不仅仅在于发现病理变化。人们已经认识到哪些病理变化具有临床意义,以及何时具有临床意义。
如果 ADL 能够帮助将该信号与背景信号分离,那么它或许能够推动阿尔茨海默病治疗——以及更广泛的长寿医学——朝着这样一个未来发展:影像学不再仅仅用于确认已经造成的损害,而是更多地用于在还有时间进行干预时解读衰老的轨迹。
🔗 https://longevity.technology/news/ai-sharpens-alzheimers-pet-readouts/
