一项新的研究发现了两种多不饱和脂肪酸,即α-桐酸(α-ESA)和α-ESA甲酯(α-ESA-me),它们在细胞培养和鼠模型中显示出衰老细胞清除活性 [1]。
抗衰老策略
细胞衰老是与衰老相关的最关键过程之一。随着年龄增长而积累的衰老细胞,其细胞周期停滞,并且对细胞死亡具有抵抗力。它们释放的炎症性衰老相关分泌表型(SASP)因子对周围的细胞环境产生有害影响,并导致许多与年龄相关的疾病,例如糖尿病、癌症、骨关节炎和阿尔茨海默病[2, 3, 4]。
靶向衰老细胞已被广泛研究作为一种抗衰老策略。尽管已取得进展并发现了一些能够清除衰老细胞的衰老细胞清除剂,但许多药物存在显著的副作用,限制了其广泛应用[5, 6, 7]。因此,仍然需要寻找更安全有效的替代方案。本研究的研究人员聚焦于脂肪酸——一种具有多种治疗作用的天然化合物[8],并探讨了其作为衰老细胞清除剂的潜力。
寻找衰老细胞清除剂
研究人员首先利用衰老细胞培养物筛选先前报道具有健康益处和膳食功能的脂肪酸[8]。他们观察到某些脂肪酸的结构特征与其衰老细胞清除活性潜力相关。
虽然衰老细胞清除活性与碳链长度之间似乎没有简单的相关性,但其他结构特征,例如脂肪酸中双键的位置和构型,似乎会影响衰老细胞清除活性,某些脂肪酸在一种构型下表现出衰老细胞清除活性,而在另一种构型下则不表现出活性。酯化和共轭作用(其中双键并非被多个单键隔开,而是以交替模式出现)也会影响衰老细胞清除活性;例如,大多数非共轭脂肪酸缺乏衰老细胞清除活性。
根据该筛选结果,我们选择了两种脂肪酸:效力最强的衰老细胞清除剂α-桐酸(α-ESA)和选择性最强的衰老细胞清除剂α-ESA甲酯(α-ESA-me),它们都是18碳共轭脂肪酸。
无毒性衰老细胞清除
研究人员在多种模型中进一步测试了已鉴定的脂肪酸,包括小鼠和由多种应激因素诱导衰老的人类细胞系。这些测试证实了α-ESA和α-ESA-me具有强大的衰老细胞清除活性;然而,不同细胞间的活性存在一定的差异。此外,两种脂肪酸之间也存在一些差异。例如,α-ESA的效力更强,诱导衰老细胞清除的速度更快,而α-ESA-me则表现出更高的选择性和更稳定、更持久的作用。
除了细胞培养实验外,研究人员还对自然衰老的小鼠(20-22个月大)进行了为期5天的治疗,测试了这两种脂肪酸的效果。结果表明,α-ESA-me在减少组织衰老方面更为有效,尤其是在肝脏和心脏组织中。在更年长的小鼠(32个月大)中,“α-ESA-me显著降低了多种组织中的衰老和SASP因子”,其中对肾脏、肝脏和肺组织的效果最为显著。
由于α-ESA-me的作用更强,因此对其进行了进一步的早衰小鼠试验。短期(3天)治疗可降低衰老标志物和SASP因子水平。长期(从10周龄开始,每周三次,持续6周)α-ESA-me治疗可降低DNA损伤、衰老和SASP标志物水平,降低衰老症状综合评分,并增加增殖细胞数量,且未观察到全身毒性作用。这些观察结果表明α-ESA-me具有清除衰老细胞和延缓衰老的潜力。
追查机制
此外,研究人员还探究了α-ESA和α-ESA-me诱导衰老细胞死亡的机制。首先,研究人员排除了细胞可能将α-ESA和α-ESA-me转化为代谢物,而这些代谢物在这些化合物的衰老细胞清除活性中发挥作用的可能性。
下一步的研究方向是α-ESA和α-ESA-me是否像大多数衰老细胞清除剂一样,通过诱导程序性细胞死亡(凋亡)发挥作用。对不同形式细胞死亡的研究表明,其作用机制并非凋亡,而是铁死亡,一种“由活性氧(ROS)积累和脂质过氧化触发的铁依赖性程序性细胞死亡”[9]。因为阻断铁死亡相关通路可以阻止α-ESA诱导细胞死亡。此外,对经处理的衰老细胞进行基因表达分析表明,α-ESA和α-ESA-me可以启动铁死亡相关的转录程序,并证实铁死亡是这些脂肪酸选择性清除衰老细胞的关键因素。
为了获得更深入的了解,研究人员采用了一种机器学习方法,结果表明,这两种α-ESA在分子通路相互作用方面与几种已知的衰老细胞清除剂(如达沙替尼和槲皮素)以及铁死亡诱导剂(如erastin和柳氮磺胺吡啶)在整体水平上相似。然而,与这些化合物相比,α-ESA具有较高的口服生物利用度和血脑屏障通透性,且全身毒性发生的可能性较低。研究结果还表明,α-ESA可能并非直接与参与细胞周期阻滞和衰老信号传导的蛋白质相互作用,而是发挥间接作用。
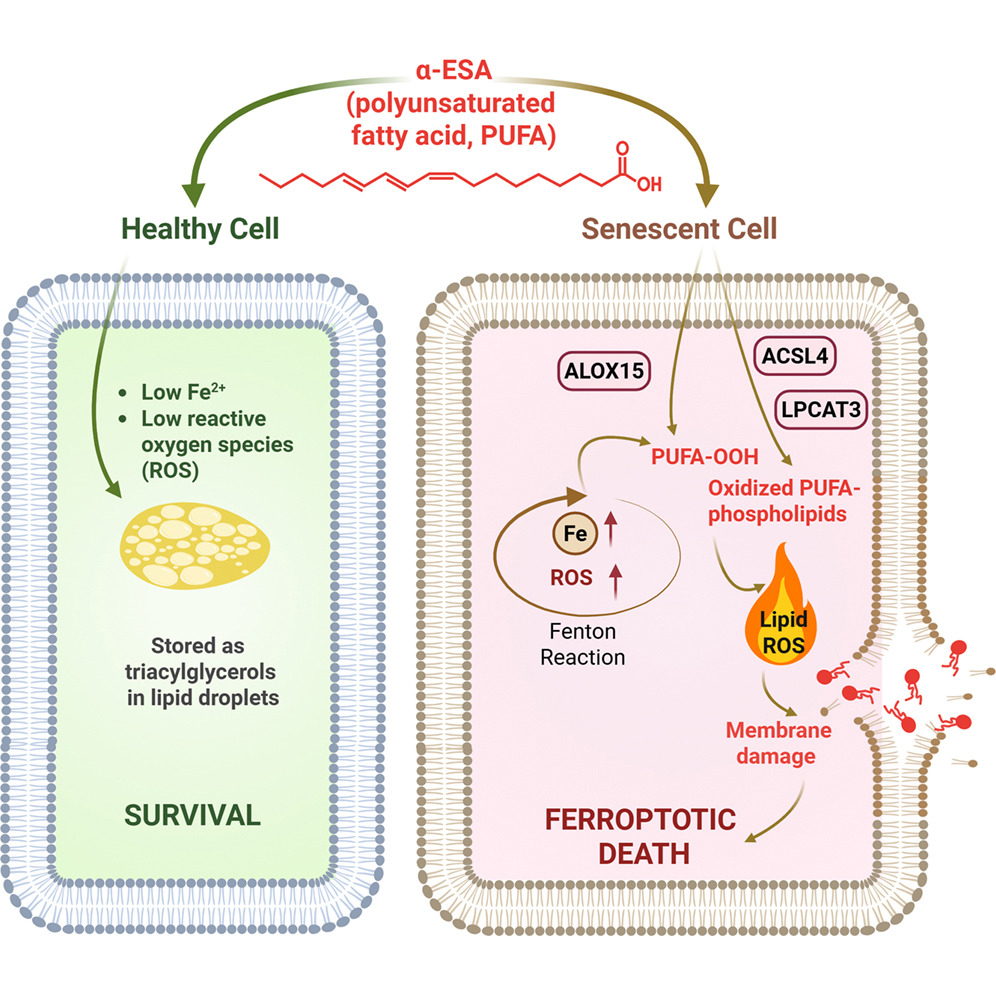
计算机模拟分析发现,铁死亡相关通路和一些蛋白质(ACSL4、LPCAT3 和 ALOX15)可能在 α-ESA 诱导的衰老细胞清除过程中发挥关键作用。抑制这些酶中的任何一种都能显著保护细胞免受 α-ESA 诱导的铁死亡,实验证实了这些酶对于 α-ESA 的衰老细胞清除作用都是必需的。
这些结果结合其他脂质组学实验,提示了α-ESA和α-ESA-me衰老细胞清除活性的可能机制。衰老细胞中亚铁离子和活性氧(ROS)的水平似乎高于非衰老细胞,而衰老细胞中铁水平的升高促进了ROS的产生。
α-ESA 和 α-ESA-me 会增强这一过程,因为它们的化学结构使其极易形成和传播自由基,从而促进脂质自由基的产生。在此过程中,α-ESA 被用作高氧化性的“燃料”,进一步被 ACSL4-LPCAT3-ALOX15 轴利用并整合到细胞膜中,导致细胞膜完整性丧失和铁死亡衰老细胞的分解。
“这篇论文首次证明,脂质可以通过触发一种独特的细胞死亡形式——铁死亡——发挥衰老细胞清除剂的作用,这与目前大多数衰老细胞清除策略截然不同,”该研究的通讯作者、明尼苏达大学医学院和生物科学学院教授、梅森衰老与代谢生物学研究所副主任保罗·罗宾斯博士表示。“我们的研究揭示了铁死亡是某些类型衰老细胞中一种独特的、可靶向的脆弱性。因此,这项工作为设计利用铁死亡生物学的衰老细胞清除疗法开辟了新的方向,并展示了特定生物活性脂肪酸的治疗潜力。”
