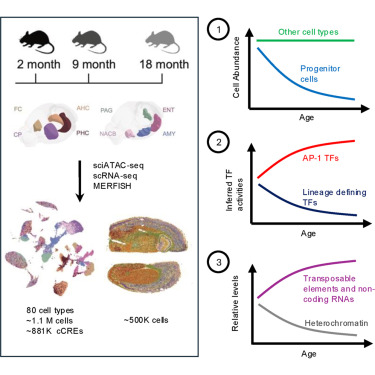
大脑衰老过程中转录调控机制的阐明仍不甚明了。本研究利用单细胞表观基因组学技术,分析了 2、9 和 18 月龄小鼠大脑八个区域的染色质可及性和基因表达谱。结果显示,除了参与神经发生和髓鞘形成的前体细胞数量显著减少外,神经元和胶质细胞的转录和染色质可及性均出现广泛且一致的年龄相关性变化。这些变化伴随着关键转录因子的失调以及由激活蛋白 1 (AP-1) 驱动的应激反应程序的转变,表明细胞身份随年龄增长而逐渐发生漂移。此外,我们还发现区域和细胞类型特异性的异染色质丢失,其特征是 H3K9me3 标记区域的可及性增加、转座元件的激活以及长链非编码 RNA 的上调,尤其是在谷氨酸能神经元中。这些发现共同揭示了与年龄相关的异染色质维持和转录调控的破坏,突显了大脑衰老过程中脆弱的脑区、细胞类型和分子通路。
🔗 https://www.cell.com/cell-reports/fulltext/S2211-1247(26)00151-8
